ปฏิวัติ ดีเอ็นเอ
แค่มองไปรอบๆ ห้องทำงานของแอนโทนี เจมส์ คุณจะเดาได้ไม่ยากว่า เขาทำงานอะไร ผนังห้องเต็มไปด้วยภาพวาดยุง และชั้นหนังสือก็เรียงรายไปด้วยหนังสือเกี่ยวกับยุง สิ่งที่แขวนถัดจากโต๊ะทำงานคือแผ่นป้ายแสดงการเจริญเติบโตทุกขั้นตอนของสิ่งมีชีวิตชนิดหนึ่ง นั่นคือยุงลายบ้าน (Aedes aegypti) “ผมหมกมุ่นเรื่องยุงมา 30 ปีแล้วครับ” เจมส์ นักพันธุกรรมโมเลกุล ที่มหาวิทยาลัยแคลิฟอร์เนียวิทยาเขตเออร์ไวน์ บอก
ทั่วโลกมียุงอยู่ราว 3,500 ชนิด แต่เจมส์ศึกษาเพียงไม่กี่ชนิด และแต่ละชนิดถูกจัดอันดับเป็นหนึ่งในสัตว์ที่ทำให้มนุษย์เสียชีวิตมากที่สุด หนึ่งในนั้นคือยุงก้นปล่อง (Anopheles gambiae) ซึ่งแพร่เชื้อปรสิตมาลาเรียที่คร่าชีวิตผู้คนหลายแสนคนในแต่ละปี อย่างไรก็ตาม งานส่วนใหญ่ของเจมส์จะมุ่งเน้นไปที่ยุงลายบ้าน นักประวัติศาสตร์เชื่อว่า ยุงมาถึงดินแดนโลกใหม่โดยติดมากับเรือขนส่งทาสจากแอฟริกาในศตวรรษที่สิบเจ็ดพร้อมกับนำโรคไข้เหลืองมาด้วย ปัจจุบัน ยุงยังเป็นพาหะของโรคไข้เลือดออกซึ่งทำให้มีผู้ติดเชื้อมากถึง 400 ล้านคนต่อปี รวมทั้งจุลชีพก่อโรคที่มีแนวโน้มเป็นภัยคุกคามมากขึ้นเรื่อยๆ อย่างชิคุนกุนยา ไข้เวสต์ไนล์ และซิกา
ในการแพร่ระบาดที่ขยายวงกว้างซึ่งเริ่มขึ้นเมื่อปีที่แล้วในบราซิล ไวรัสซิกาดูเหมือนจะเป็นสาเหตุของความผิดปกติทางระบบประสาทหลายชนิด รวมทั้งความผิดปกติหายากชนิดหนึ่งที่เรียกว่า ภาวะศีรษะเล็ก (microcephaly) ซึ่งทำให้ทารกมีศีรษะเล็กผิดปกติและสมองมีพัฒนาการล่าช้า
เป้าหมายของเจมส์ตลอดระยะเวลาที่ผ่านมาคือ การหาหนทางปรับแต่งยีนของยุงเพื่อให้มันไม่สามารถแพร่เชื้อเหล่านั้นได้อีกต่อไป กระทั่งเมื่อไม่นานมานี้ ความพยายามดังกล่าวยังเป็นได้เพียงแค่แนวคิดทางทฤษฎีที่ไม่ค่อยมีคนพูดถึงหรือได้รับสนใจ ทว่าการรวมเทคโนโลยีใหม่ระดับปฏิวัติวงการเรียกว่า คริสเปอร์-แคสไนน์ (CRISPR-Cas9) เข้ากับระบบทางธรรมชาติที่เรียกว่า ยีนไดรฟ์ [gene drive – ดีเอ็นเอที่ถ่ายทอดไปสู่รุ่นลูกหลานได้ “ถี่” กว่าปกติ] ทำให้ทฤษฎีที่ว่ากำลังกลายเป็นความจริงอย่างรวดเร็ว
คริสเปอร์หยิบยื่นอำนาจใหม่ใส่ในมือมนุษย์ เป็นครั้งแรกที่นักวิทยาศาสตร์สามารถปรับเปลี่ยน ลบ และจัดเรียงดีเอ็นเอของสิ่งมีชีวิตเกือบทั้งหมดรวมทั้งมนุษย์ได้อย่างรวดเร็วและแม่นยำ ในช่วงสามปีที่ผ่านมา เทคโนโลยีได้เปลี่ยนโฉมหน้าชีววิทยา นักวิจัยในห้องปฏิบัติการทั่วโลกเริ่มใช้คริสเปอร์กับตัวอย่างสัตว์เพื่อแก้ไขข้อบกพร่องทางพันธุกรรมที่สำคัญ รวมทั้งการกลายพันธุ์ซึ่งทำให้เกิดโรคกล้ามเนื้อเสื่อมหรือเจริญผิดเพื้ยน (muscular dystrophy) โรคซิสติกไฟโบรซิส (cystic fibrosis) และรูปแบบหนึ่งของโรคตับอักเสบ
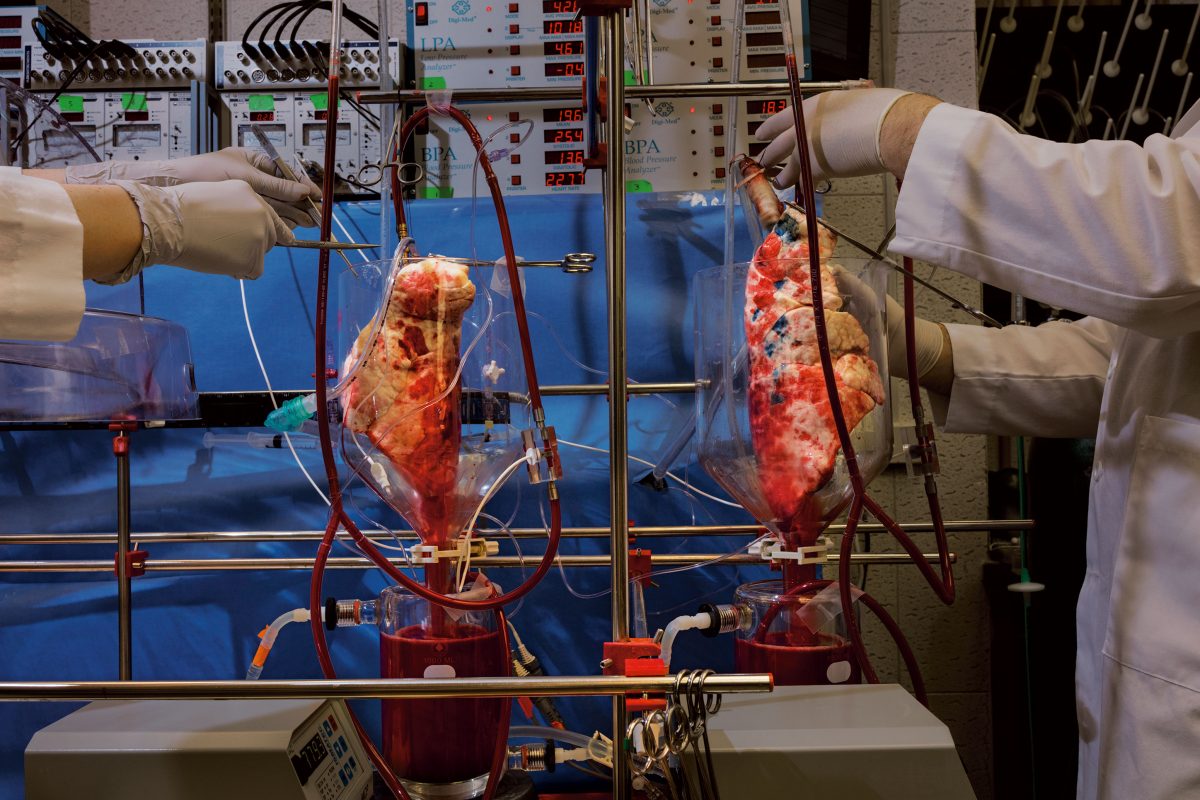
ในการทดลองหลายครั้ง นักวิทยาศาสตร์ใช้คริสเปอร์เพื่อกำจัดไวรัสในหมูซึ่งขัดขวางการปลูกถ่ายอวัยวะของหมูให้กับมนุษย์ ขณะที่นักนิเวศวิทยากำลังหาวิธีใช้เทคโนโลยีนี้เพื่อปกป้องสิ่งมีชีวิตชนิดต่างๆที่ใกล้สูญพันธุ์ และนักชีววิทยาพืชที่วิจัยพืชผลทางการเกษตรหลายชนิดเริ่มลงมือกำจัดยีนที่ดึงดูดแมลงศัตรูพืช โดยใช้ชีววิทยาแทนที่จะพึ่งพาสารเคมีต่างๆ คริสเปอร์จึงอาจช่วยให้เราลดการพึ่งพายาฆ่าแมลงต่างๆ ซึ่งเป็นพิษได้อีกด้วย

ไม่มีการค้นพบทางวิทยาศาสตร์ใดๆ ในช่วงร้อยปีที่ผ่านมาที่จะศักยภาพในการรักษาโรคต่างๆ ในอนาคตได้มากกว่านี้และยังก่อให้เกิดคำถามทางจริยธรรมได้มากกว่านี้อีกแล้ว คำถามที่เป็นปัญหามากที่สุดคือ ถ้ามีการนำคริสเปอร์ไปใช้ในการปรับแต่งเซลล์ต้นกำเนิดเซลล์สืบพันธุ์ของตัวอ่อนมนุษย์ (germ line) ซึ่งเป็นเซลล์ที่บรรจุสารพันธุกรรม (genetic material) ที่ถ่ายทอดไปสู่รุ่นต่อไปได้ไม่ว่าจะเพื่อแก้ไขข้อบกพร่องทางพันธุกรรมหรือเพิ่มคุณลักษณะหนึ่งๆ ที่ต้องการ ผลการปรับแต่งดังกล่าวจะส่งผ่านไปสู่รุ่นลูกหลานของพวกเขาอย่างถาวร ผลกระทบทั้งหมดในอนาคตนั้นยากที่จะทำนาย หรือไม่สามารถทำนายได้เลย
เอริก แลนเดอร์จากมหาวิทยาลัยฮาร์วาร์ดและสถาบันเอ็มไอที ซึ่งเคยเป็นผู้นำโครงการจีโนมมนุษย์ (Human Genome Project) บอกว่า “นี่คือเทคโนโลยีที่ยอดเยี่ยมและมีประโยชน์หลายประการ แต่ถ้าคุณจะทำอะไรบางอย่างที่สร้างผลกระทบใหญ่หลวงและเป็นการถาวรอย่างการเขียนเซลล์ต้นกำเนิดเซลล์สืบพันธุ์ของตัวอ่อนมนุษย์ ขึ้นใหม่ คุณต้องอธิบายได้ว่า มีเหตุผลที่มีน้ำหนักพอที่จะทำเช่นนั้น และต้องบอกได้ด้วยว่า สังคมได้ตัดสินใจเลือกเดินเส้นทางนั้น พูดง่ายๆ คือถ้าไม่มีฉันทามติในวงกว้าง สิ่งนี้คงไม่มีวันเกิดขึ้นครับ”
แลนเดอร์บอกผมว่า “นักวิทยาศาสตร์ยังไม่ได้ข้อยุติร่วมกันในการตอบคำถามเหล่านี้ ”
คริสเปอร์-แคสไนน์มีองค์ประกอบสองส่วน ส่วนแรกคือเอนไซม์แคสไนน์ (Cas9 enzyme) ซึ่งทำหน้าที่เป็น “มีดผ่าตัด” ภายในเซลล์เพื่อตัดดีเอ็นเอ (ในธรรมชาติแบคทีเรียใช้เอนไซม์แคสไนน์ในการตัดและหยุดยั้งการทำงานของรหัสพันธุกรรมของไวรัสผู้บุกรุก) อีกส่วนหนึ่งคืออาร์เอนเอนำทาง (RNA guide) ซึ่งเป็นตัวนำมีดผ่าตัดไปสู่นิวคลีโอไทด์อันเป็นหน่วยย่อยทางเคมีของดีเอ็นเอจำเพาะเจาะจงที่ต้องการตัด ส่วนคำว่าคริสเปอร์ย่อมาจากศัพท์เทคนิคที่เข้าใจยาก นั่นคือ “กลุ่มของดีเอ็นเอซ้ำๆ กลับไปมาที่แทรกอยู่เป็นระยะอย่างสม่ำเสมอ” (Clustered Regularly Interspaced Short Palindromic Repeats: CRISPR)
ความถูกต้องแม่นยำของอาร์เอนเอนำทางนั้นน่าทึ่งมาก อาร์เอนเอนำทางสามารถค้นหาจุดที่ต้องการตัดได้อย่างแม่นยำ นักวิทยาศาสตร์สามารถส่งชุดดีเอ็นเอสังเคราะห์เพื่อการแทนที่ (synthetic replacement part) ไปสู่ตำแหน่งใดๆ ในจีโนมซึ่งสร้างขึ้นจากนิวคลีโอไทด์หลายพันล้านหน่วย เมื่อคริสเปอร์เดินทางถึงจุดหมายของมัน เอนไซม์แคสไนน์จะตัดชุดลำดับดีเอ็นเอที่ไม่ต้องการออกไป และเซลล์จะเชื่อมส่วนที่ตัดขาดออกด้วยการสอดเติมสายโซ่ของนิวคลีโอไทด์ที่ส่งมาพร้อมกันในชุดของคริสเปอร์ (CRISPR package)
เมื่อการระบาดของโรคไข้ซิกาในเปอร์โตริโกยุติลง ศูนย์ควบคุมและป้องกันโรคของสหรัฐฯ หรือซีดีซี (Centers for Disease Control and Prevention: CDC) ประเมินว่า ชาวเปอร์โตริโกอย่างน้อยหนึ่งในสี่ของประชากร 3.5 ล้านคนอาจสัมผัสเชื้อไข้ซิกานั่นหมายความว่า หญิงตั้งครรภ์หลายพันคนมีแนวโน้มที่จะกลายเป็นผู้ติดเชื้อ
ขณะนี้การต่อสู้กับไวรัสซิกาที่มีประสิทธิภาพเพียงอย่างเดียวอาจเป็นการ “อาบ” เกาะทั้งเกาะด้วยยาฆ่าแมลง เจมส์และคนอื่นๆ เชื่อว่า การปรับแต่งพันธุกรรมยุงด้วยคริสเปอร์และการใช้ยีนไดร์ฟเพื่อเปลี่ยนยีนของยุงอย่างถาวรช่วยให้เรามีหนทางแก้ปัญหาที่ดีกว่าเดิม
ยีนไดร์ฟมีอำนาจที่จะเอาชนะกฎของการถ่ายทอดทางพันธุกรรรมแบบดั้งเดิมได้ ตามปกติแล้ว ผู้สืบสายโลหิตที่เกิดจากการสืบพันธุ์แบบอาศัยเพศของสัตว์ใดๆ จะได้รับสำเนายีนจากพ่อแม่อย่างละหนึ่งชุด หรือมีโอกาสในการส่งผ่านยีนหนึ่งๆ เท่ากับร้อยละ 50 อย่างไรก็ตาม ยีนบางส่วนจะเป็นยีน “เห็นแก่ตัว” (selfish) กล่าวคือ วิวัฒนาการทำให้ยีนเหล่านี้มีโอกาสถ่ายทอดมากกว่าร้อยละ 50 ในทางทฤษฎี นักวิทยาศาสตร์อาจรวมคริสเปอร์กับยีนไดร์ฟเข้าด้วยกันเพื่อดัดแปลงรหัสพันธุกรรมของชนิดพันธุ์หนึ่งๆ ด้วยการติดชุดลำดับดีเอ็นเอ (DNA sequence) ที่ต้องการลงบนยีนที่ต้องการถ่ายทอด ก่อนจะปล่อยให้สัตว์จับคู่กันตามธรรมชาติ การใช้เครื่องมือทั้งสองอย่างร่วมกันอาจบังคับให้ประชากรทั้งกลุ่มมีลักษณะทางพันธุกรรมใดๆ ที่ต้องการได้
เมื่อปีที่แล้ว ผลการวิจัยซึ่งได้รับการตีพิมพ์ในวารสาร การดำเนินงานของสถาบันวิทยาศาสตร์แห่งชาติ (Proceedings of the National Academy of Sciences) เจมส์ใช้คริสเปอร์ในการออกแบบพันธุกรรมยุงก้นปล้อง Anopheles รุ่นใหม่ที่ทำให้พวกมันไม่สามารถแพร่กระจายเชื้อปรสิตมาลาเรียได้
เจมส์บอกว่า “ ผมเคยทำงานหามรุ่งหามค่ำ แต่ไม่มีใครเห็นอยู่หลายสิบปี แต่เดี๋ยวนี้ไม่ใช่แล้ว โทรศัพท์ผมดังไม่หยุดมาหลายสัปดาห์แล้วครับ”
การต่อสู้กับยุงลายบ้าน (Aedes aegypti) ซึ่งเป็นพาหะนำโรคหลายชนิดอาจต้องใช้วิธีการจัดการที่ต่างออกไปเล็กน้อย เจมส์บอก ผมว่า “สิ่งที่คุณจำเป็นต้องทำคือการออกแบบยีนไดร์ฟที่ทำให้ยุงเป็นหมัน การสร้างยุงที่ต้านทานต่อเชื้อไวรัสซิกาจะไม่มีประโยชน์ ถ้ามันยังสามารถแพร่เชื้อโรคไข้เลือดออกและโรคอื่นๆได้”
ในการต่อสู้กับโรคไข้เลือดออก เจมส์และเพื่อนร่วมงานออกแบบชุดคริสเปอร์ที่สามารถกำจัดยีนธรรมชาติจากพ่อแม่ยุงในธรรมชาติ และทดแทนด้วยยีนใหม่ซึ่งจะทำให้ยุงรุ่นลูกเป็นหมัน ถ้ามีการปล่อยยุงที่ได้รับตัดแต่งพันธุกรรมเหล่านี้จำนวนมากพอออกไปให้จับคู่ผสมพันธุ์ในธรรมชาติ ภายในไม่กี่ชั่วรุ่นให้หลัง (ซึ่งปกติยุงแต่ละรุ่นจะมีอายุเแค่สองหรือสามสัปดาห์เท่านั้น) ประชากรยุงทั้งชนิดก็จะมียีนที่ได้รับการออกแบบใหม่อยู่ในตัว
กระนั้น เจมส์ตระหนักดีว่า การปล่อยรูปแบบการกลายพันธุ์ซึ่งออกแบบให้แพร่กระจายอย่างรวดเร็วทั่วทั้งกลุ่มประชากรในธรรมชาติอาจนำไปสู่ผลที่ไม่คาดคิดตามมา และอาจไม่ง่ายที่จะย้อนกระบวนการกลับไป “ความเสี่ยงจากการปล่อยแมลงที่ได้รับการตัดแต่งพันธุกรรมในห้องปฏิบัติการมีแน่นอนครับ” เขายอมรับ “แต่ผมคิดว่าถ้าเราไม่ทำอะไรเลย ความเสี่ยงจะยิ่งมีมากกว่าครับ”
เรื่อง ไมเคิล สเปกเตอร์
ภาพถ่าย เกรก จีราร์
อ่านเพิ่มเติม